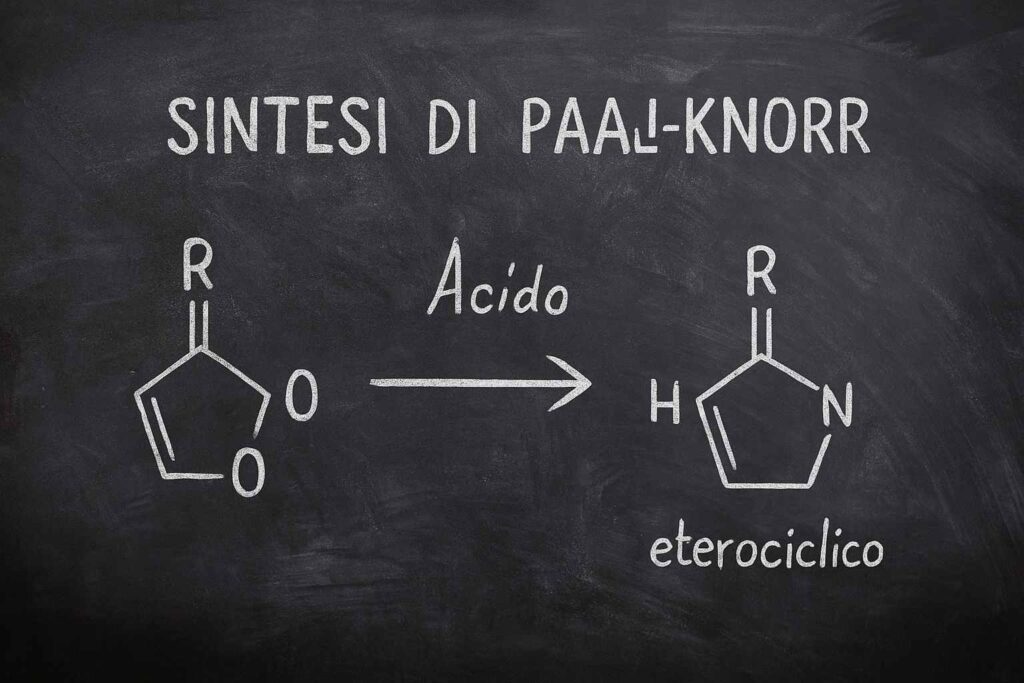
Sintesi di Paal-Knorr: come funziona e perché è fondamentale nella chimica eterociclica
Nel 1884 due chimici tedeschi definirono il processo oggi noto come sintesi di Paal-Knorr per sintetizzare composti organici eterociclici. Gli scienziati di cui parliamo erano Carl Paal e Ludwig Knorr, che si occuparono soprattutto dello studio di farmaci. Possiamo ad esempio ricordare il fenazone, composto con proprietà analgesico e spasmolitico conosciuto anche come antipirina.
Tramite l’insieme di reazioni che compone il processo è possibile ottenere come prodotti il furano, il pirrolo e il tiofene, partendo dalla stessa materia prima. Queste tre molecole hanno tutte la particolarità di presentare a livello strutturale un anello eterociclico, dove oltre al carbonio possiamo trovare azoto (N), ossigeno (O) o zolfo (S).
La sintesi di Paal-Knorr per il furano
Come vale anche per il pirrolo e il tiofene questa reazione sfrutta come molecola di partenza gli 1,4-dichetoni. Si sfrutta la catalisi acida per ottenere il furano, quindi c’è bisogno di avere a disposizione un ambiente con un acido forte. Quello che si sfrutta più di frequente è l’acido solforico (H2SO4), o in alternativa l’acido cloridrico (HCl).
L’acido forte causa una protonazione a livello di uno dei gruppi carbonile dell’1,4-dichetone e si forma un enolo. Questo composto ha un gruppo alchenico e uno ossidrilico, e interagisce con il secondo gruppo carbonilico causando la ciclizzazione della molecola. Si ottiene così un emiacetale, prima che la sintesi di Paal-Knorr giunga a conclusione con la disidratazione di questa molecola.
Come agente disidratante per ricavare il furano si utilizza spesso il cloruro di zinco (ZnCl2), un sale igroscopico spesso usato anche come acido di Lewis. Il prodotto finale di questo processo di sintesi presenta un anello eterociclico aromatico con un atomo di ossigeno come eteroatomo (formula bruta C4H4O). In alternativa il furano si può ottenere anche attraverso la distillazione del legno.
Questo composto si può facilmente ridurre per ottenere una molecola più stabile, ovvero il tetraidrofurano (C4H8O). Si tratta di un etere ciclico che risulta solubile in acqua e stabile in ambiente basico ed è molto usato come solvente a livello industriale. Quando si forma in seguito alla cottura degli alimenti però si considera un contaminante oltre che potenziale cancerogeno.
Come ricavare il pirrolo
Passiamo a un’altra variante della sintesi di Paal-Knorr, quella che produce un anello aromatico eterociclico che contiene azoto. Per ottenerlo dobbiamo sfruttare sempre un 1,4-dichetone da far reagire con dell’ammoniaca (NH3) o un’ammina primaria (NRH2). Quando si usa un’ammina primaria questa interagiscono uno dei carbonili formando un intermedio di reazione detto emiamminale.
Il gruppo amminico di questa molecola attacca poi l’altro gruppo C=O formando un secondo composto intermedio ciclico. Anche in questo caso la sintesi si conclude con la perdita di una molecola d’acqua. Si ottiene così un pirrolo con un sostituente legato all’azoto ma se l’1,4-dichetone reagisce con l’ammoniaco il prodotto finale non presenta sostituenti (C4H5N).
Il pirrolo puro a temperatura ambiente appare come un liquido trasparente, facilmente infiammabile e di consistenza oleosa. Si scioglie facilmente in etere o alcool mentre non è solubile in acqua. La prima volta che lo si produsse in un laboratorio chimico fu nel 1860, ma la reazione sfruttata all’epoca non fu la sintesi di Paal-Knorr, ma la pirolisi di un sale d’ammonio.
Il pirrolo si sfrutta molto per ottenerne dei derivati spendibili come principi attivi all’interno di farmaci per contrastare le infezioni fungine. Al momento sono allo studio anche possibili applicazioni in medicinali antibatterici per contrastare la proliferazione di ceppi resistenti agli antibiotici più comuni. Vale sia per le specie Gram-positive che per quelle Gram-negative.
Il tiofene dalla sintesi di Paal-Knorr
Come negli altri due processi ci serve un ambiente acido, con acido cloridrico o solforico. Il tiocarbonile formato diventa un enotiolo che in seguito ciclizza. Successivamente grazie al potere disidratante dei composti contenenti zolfo questo intermedio perde una molecola d’acqua. Questo rimuove l’-OH legato all’atomo di zolfo crea un doppio legame all’interno dell’anello eterociclico.
Il tiofene in natura si trova spesso all’interno del benzene, dove rappresenta un’impurità. A temperatura ambiente è un liquido incolore, leggermente più denso dell’acqua e come il pirrolo non si scioglie in soluzione acquosa. Risulta invece facilmente solubile all’interno di solventi come l’etanolo (C2H6O) oppure l’etere dietilico (C4H10O).
In campo industriale il tiofene non trova larga applicazione, ma si può usare per ottenere dei derivati che invece risultano utili in vari settori. Per esempio nelle aziende che producono coloranti o detergenti, e sono allo studio anche altre applicazioni. Tuttavia è considerato una sostanza inquinante se dispersa nell’atmosfera, e se respirato causa irritazione alle vie respiratorie, oltre a irritare gli occhi.
Le limitazioni dell’uso di questo processo
Nel momento in cui divenne nota era innegabile che la sintesi di Paal-Knorr presentasse diversi vantaggi. Prima di tutto la sua versatilità, dato che permetteva di ottenere diverse classi di composti, ma è innegabile che per avvenire richieda condizioni complesse da realizzare. C’è bisogno infatti di lasciare a lungo i precursori in ambiente acido e riscaldato, che porta spesso a denaturazione dei gruppi funzionali.
Dato questo difetto che rischia di rendere inefficace il processo chimico si sta studiando come migliorare e rendere più efficiente il sistema. La sfida principale si è rivelata renderlo più sostenibile, meno tossico per l’ambiente oltre che più rapido. Ottenere composti organici con metodi avanzati è essenziale per le ricerche in corso in ambito farmaceutico.