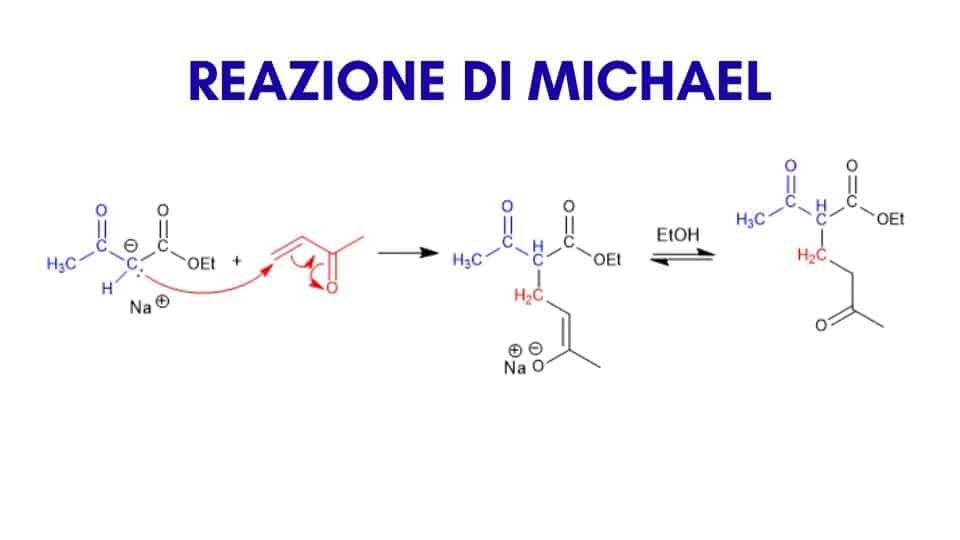
L'addizione nucleofila con la reazione di Michael
In Chimica Organica utilizziamo la reazione di Michael per ottenere un’addizione nucleofila che porta alla formazione di un legame fra due atomi di carbonio (C – C). La scoperta di questo processo risale al 1887 e si deve al chimico americano Arthur Michael, docente all’Università di Harvard. Uno dei suoi vantaggi è quello di non richiedere condizioni sperimentali complesse.
All’interno di questo meccanismo di addizione intervengono l’enolato di un derivato metilico e un composto carbonilico α β -insaturo. Questa seconda molecola ha un doppio legame coniugato con un gruppo funzionale che può variare. Può trattarsi di un chetone (C=O)) come di un’aldeide (−CH=O) o di un’estere (C=OOR).
Il meccanismo di reazione di Michael
Si inizia con i due composti indicati prima, un enolato metilico che nella reazione si indica come donatore di Michael e un composto carbonilico α-β insaturo che costituisce l’accettore di Michael. Il prodotto che otterremo alla fine sarà un 1,5-carbonile, o addotto di Michael.
A questo punto si verifica l’addizione nucleofila 1.,4 che va a formare un intermedio di reazione, a cui poi si va a legare un atomo di idrogeno estratto dalla base protonata. In questo modo si arriva al prodotto finale con la formazione del legame fra due atomi di carbonio. A quanto racconta la storia a ispirare il chimico statunitense fu una pubblicazione di circa 3 anni prima. un lavoro a firma Conrad & Kuthzeit.
Perché questo processo di addizione nucleofila proceda facilmente si possono utilizzare come prodotti di partenza enolati che derivino da composti con pKa inferiore a 4. La reazione esaminata si può utilizzare anche insieme a un altro processo creando l’anellazione di Robinson, che produce chetoni α,β insaturi ciclici a sei atomi di carbonio.
La reazione scoperta da sir Robert Robinson
Famoso chimico inglese insignito del premio Nobel per la Chimica nel 1947, creò il processo di anellazione che porta il suo nome mentre lavorava a Oxford.
Per creare chetoni α combinò la reazione di Michael con un processo di condensazione aldolica per ottenere dei composti definiti come sistemi cicloesenonici. L’anellazione di Robinson ha importanti applicazioni in Medicina, per esempio per produrre il cortisone.
La reazione inizia in ambiente controllato e in presenza di basi. Si parte da un chetone che presenta un atomo di idrogeno sul C in alfa sul carbonile e da un chetone α,β insaturo. Come prima si ha la deprotonazione e la formazione di un enolato, che subisce un’addizione nucleofila 1,4 per poi ricevere un idrogeno e diventare un dichetone.
A questo punto la reazione di Michael termina e si procede con il secondo processo dell’anellazione di Robinson. La condensazione aldolica si svolge a livello intramolecolare, sempre favorita dall’ambiente basico. Infine si elimina un gruppo OH formando il cicloesanone α,β e una molecola d’acqua.
La condensazione aldolica è possibile anche per le aldeidi, ma l’equilibrio di reazione è più spostato verso la formazione dell’aldolo che non verso il reagente. La presenza di una base forte come catalizzatore nel caso dei chetoni è dovuto al fatto che invece nel loro caso l’equilibrio favorisce la formazione dei chetoni verso i chetoli.
La sonochimica e la reazione di Michael
Si definisce sonochimica e il suo fine è quello di intensificare le reazioni chimiche, in particolare quelle di sintesi e di catalisi. Con queste onde sonore si può rendere un processo più veloce, più efficiente o cambiare le condizioni necessarie perché avvenga.
Studi recenti hanno mostrato che tra i processi di sintesi che possono trarre vantaggio dalla sonochimica c’è proprio la reazione di Michael. In particolare si è osservato un aumento della velocità di reazione oltre che una resa più efficace rispetto alle condizioni standard. Il processo con gli ultrasuoni inoltre risulta più sostenibile, semplice e sicuro per gli operatori.
Per catalizzare l’addizione nucleofila oltre alla sonochimica una ricerca svolta nel 2002 da Martin-Aranda e il suo team aveva utilizzato anche argille basiche di imidazolo. L’imidazolo (C3H4N2) è una molecola organica eterociclica aromatica.
Si utilizza anche per svolgere un’analisi qualitativa dell’acqua sfruttando il metodo di Karl Fischer.
Un’analogia da ricordare
Come la reazione di Michael, si tratta di un processo di addizione nucleofila. Intervengono come reagenti un silil-enol-etere e un composto α,β insaturo catalizzata dalla presenza di un acido di Lewis. Per ricavare i silil-enol-eteri si utilizzano dei chetoni da trattare con trimetil-silil-cloruro in presenza di una base forte.
Attraverso l’addizione di Mukaiyama-Michael si possono ottenere strutture molecolari complesse. Più spesso la si trova riportata come addizione aldolica di Mukaiyama, e come acido di Lewis per catalizzarla si utilizza spesso il cloruro di titanio (TiCl4). Questa reazione non è reversibile e avviene in condizioni semplici da gestire.
Le applicazioni della reazione di Michael
L’ibrutinib si usa oggi per esempio per trattare il linfoma mantellare e la leucemia linfocitica cronica (CLL) quando compaiono delle recidive dopo un primo trattamento.