Il principio di De Broglie e la doppia natura della materia
Dalla scoperta della doppia natura della luce già di per sé rivoluzionaria nacque il principio di De Broglie, noto anche con il nome di onda di materia. In pratica la sua teoria si basava sullo stesso principio del dualismo onda-particella e supponeva che anche la materia avesse una doppia natura: corpuscolare e ondulatoria.
La scoperta del fotone avvenne verso la fine del 1800, ma fu solo nel 1924 che questo giovane fisico francese decise di formulare la sua ipotesi. Per la precisione la scrisse all’interno della propria tesi di dottorato, intitolata Recherches sur la Théorie des Quanta. Questa fu solo il primo di una serie di pubblicazioni sulla Meccanica Quantistica che arrivarono negli anni seguenti.
Le basi dell’ipotesi di De Broglie
Prima della tesi di dottorato del 1924 Louis-Victor Pierre Raymond De Broglie si era interessato allo studio dei raggi X e all’effeto fotoelettrico, interpretato secondo la teoria dei quanti. Dopodiché a partire dal 1922 iniziò a dedicarsi alle possibili implicazioni della teoria corpuscolare della luce. In particolare presentò al Journal Physique una derivazione della legge di Wien per il corpo nero dove trattava i quanti di luce come particelle.
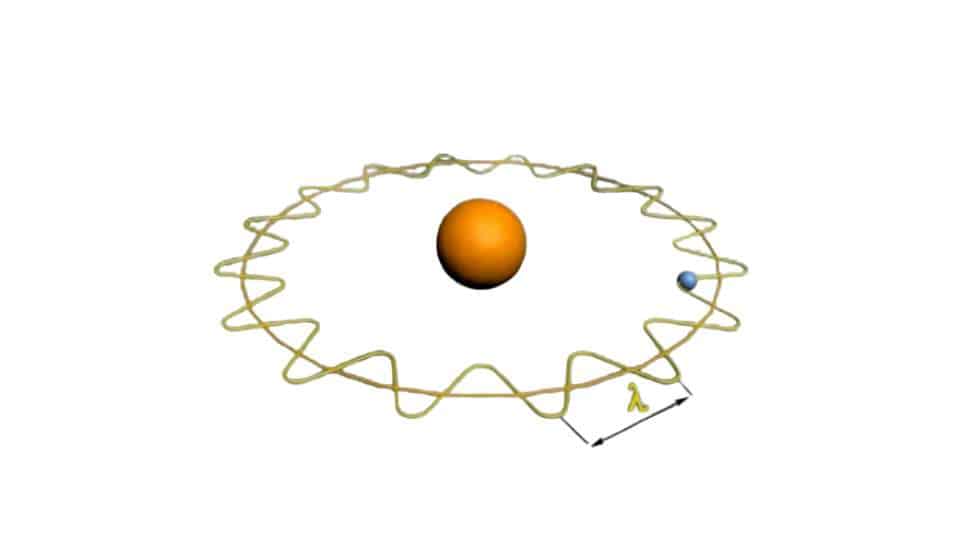
Pur se spiegata accuratamente all’interno della tesi, le basi dell’ipotesi di De Broglie apparvero per la prima volta su delle note scritte del 1923 proposte per la pubblicazione su una rivista scientifica. Erano tre in tutto, di cui la prima forniva un’interpretazione semplice per la stabilità quantistica dei livelli atomici dell’atomo. Stabiliva una relazione tra la velocità del moto di un particella e la velocità di fase di un’onda.
All’interno della seconda nota il fisico propose invece una teoria sui fenomeni della diffrazione e dell’interferenza fra le onde luminose che risultasse compatibile con l’esistenza dei fotoni. Considerando queste particelle stabilì che ciascuna di loro si muovesse lungo un’onda ad essa associata, che rappresenta una traiettoria “pilota”.
Rimane la terza nota, che stabiliva come le sue proprie ipotesi potessero condurre alla funzione di Planck per lo studio del corpo nero. Si trattò di tre note rivoluzionarie ma che all’epoca destarono ben poco interesse. Nella tesi di dottorato le presentò in maniera più estesa (sette capitoli), ma nominando l’onda di materia solo al capitolo 4.
Cos’è l’onda di materia e la sua formula
Come accennato l’idea alla base dell’ipotesi di De Broglie fu il fatto che ogni forma di materia possedesse una doppia natura, una come onda e una come particella. Per una qualsiasi particella possiamo quindi ricavare un’onda con lunghezza d’onda λ data dalla formula h/m · v. In questo formula nel dettaglio:
- h è la costante di Planck, una delle costanti fondamentali per la Meccanica Quantistica che vale 6,626 x 10-34 J·s.
- m indica la massa della particella che stiamo considerando e quella dell’elettrone è 9,11 x 10-31 kg.
- v corrisponde alla velocità della particella, e si esprime in m/s.
Secondo l’ipotesi di De Broglie vediamo che il valore della lunghezza d’onda λ aumenta quando la massa diminuisce. Di conseguenza λ e m sono fra loro in un rapporto di proporzionalità inversa. Per questo motivo non si può applicare questa ipotesi a oggetti macroscopici perché avrebbero valori di lunghezza d’onda infinitesimi.
Qualche esempio pratico sull’ipotesi di De Broglie
Se invece partendo dalla lunghezza d’onda dovessimo ricavare la velocità della particella in movimento dovremmo usare la formula inversa v = h/mλ. Quindi supponendo di avere un elettrone che si muove lungo un’onda pilota con lunghezza d’onda pari a 6,2 x 10-12 m. Sostituendo i dati otterremo che la velocità è pari a 6,626 x 10-34 Js/(9,11 x 10-31 kg x 6,2 x 10-12 m) = 1,17 x 108 m/s.
Dall’onda di materia alla teoria di Bohm
Presentata nel 1927 oggi è attribuita a David Joseph Bohm, che la rielaborò nel 1952 dandole la forma definitiva che compare sui libri di Fisica.