Composti aromatici: quali sono e come riconoscerli
Quando ci si prepara per il test di ammissione a Medicina e Odontoiatria i composti aromatici sono uno degli argomenti possibili nelle domande di Chimica. Si tratta di una categoria di idrocarburi definiti in questo modo per il loro odore intenso, dolciastro, e il fatto che evaporano facilmente all’aria diffondendosi nell’ambiente.
Oltre al loro aroma anche la struttura che hanno li differenzia dagli altri idrocarburi (come gli alcheni) e fornisce loro una reattività particolare, diversa dai composti alifatici. Le loro molecole sono composte da anelli aromatici, ma non vanno confuse con i composti ciclici semplici come i cicloalcheni, che presentano comunque legami doppi.
Cosa sono i composti aromatici: definizione e legami
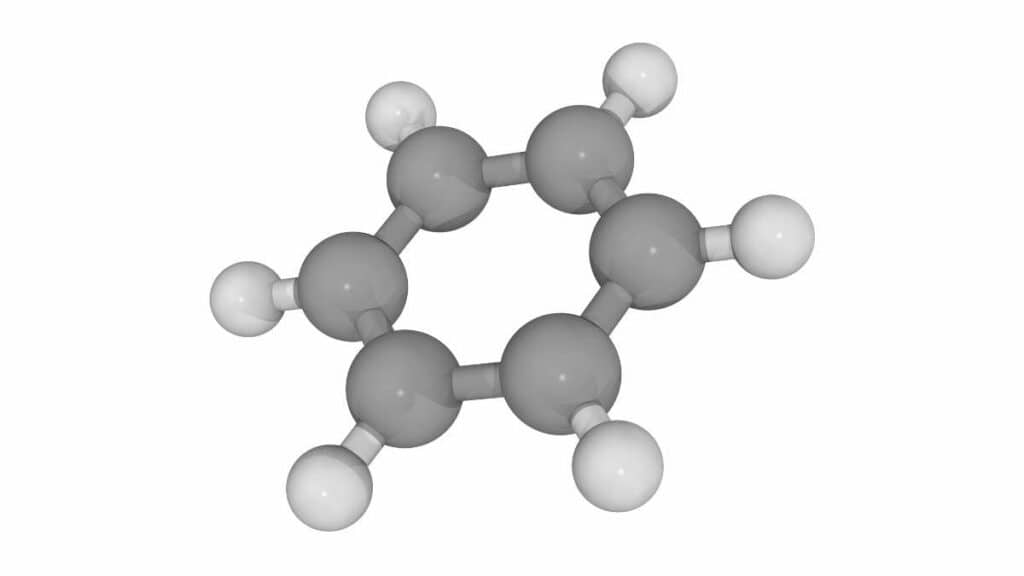
In Chimica si definisce composto aromatico quando la struttura di una molecola al suo interno include uno o più anelli aromatici. L’esempio più usato è quello del benzene (C6H6) dato che è composto da un unico anello di 6 atomi di carbonio. Al suo interno questi atomi sono uniti fra loro da doppi legami e legano un atomo di idrogeno (H).
Per semplificare si può anche dire che gli areni o composti aromatici siano le molecole organiche che hanno una struttura simile al benzene. L’anello arenico è reso possibile dall’ibridazione sp2 degli orbitali del carbonio che quindi si uniscono in questa struttura con sei legami π, come se si trattasse di tre molecole di etilene unite fra loro.
Nel caso del benzene non c’è una struttura definitiva della molecola che invece oscilla tra le sue due forme limite di risonanza. La molecola vera è un ibrido tra le due, perché risulta più stabile di entrambe. Inoltre a lunghezza dei legami interni all’anello arenico è a metà tra quella di un legame semplice e uno doppio.
A livello di reattività gli idrocarburi aromatici anziché reazioni di addizione elettrofila danno luogo a sostituzione. La dinamica vede infatti l’elettrofilo sostituire uno dei sei idrogeni legati ciascuno a un diverso atomi di carbonio. Rispetto alle molecole non aromatiche inoltre si tratta di composti più stabili, che liberano meno energia durante la combustione.
Le quattro regole dell’aromaticità
Per essere sicuri di avere davanti una molecola che rientra nella categoria dei composti aromatici ci sono 4 caratteristiche che deve presentare. Si definiscono le 4 regole dell’aromaticità:
- La molecola è ciclica, ovvero si presenta con una struttura chiusa su sé stessa, come per il benzene. Dato che questo è l’anello aromatico d’esempio tutti i suoi derivati sono senza dubbio idrocarburi aromatici. Un esempio è il toluene, dove un atomo di idrogeno del benzene risulta sostituito da un gruppo metilico (-CH₃).
- Nella struttura dei composti aromatici gli orbitali p degli atomi sono paralleli fra di loro e risultato perpendicolari alla molecola stessa. Si tratta del legame π già nominato, dove i due orbitali bilobati si sovrappongono lateralmente anziché in modo frontale come nel legame σ.
- La molecola soddisfa la regola di Hückel. Si tratta di un metodo proposto dal famoso chimico tedesco per capire con un semplice calcolo se si sia di fronte a un composto aromatico. Essa prevede che gli elettroni del legame π debbano essere pari a 4n + 2. Il valore di n deve essere un numero naturale superiore a zero. Nel caso del benzene ad esempio sono 6 (4 x 1 + 2 = 6).
- La struttura del composto deve risultare completamente coniugata. In ogni punto di unione dell’anello (fra due carboni) deve essere presente l’ibridazione vista in precedenza.
Composti aromatici più comuni
Ci sono anche molecole organiche formate da più anelli: i composti aromatici policiclici. L’esempio standard è quello del bifenile, dove si trovano due anelli uniti da un legame sigma e la sua formula bruta è (C6H5)2. Lo si può ricavare dal petrolio greggio o dal catrame per distillazione e torna utile sia per produrre materie plastiche che per la formulazione di alcuni pesticidi.
Ci sono poi i composti eterociclici che hanno la particolarità di avere all’interno dell’anello aromatico un atomo diverso dal carbonio. In particolare si può trovare un azoto (N), di zolfo (S) oppure di ossigeno (O). Possiamo citare il pirrolo (C4H5N), che si presenta come un liquido altamente infiammabile che si ossida rapidamente all’aria passando da trasparente a giallo-bruno.
Molto simile al pirrolo ma con un atomo di zolfo al posto dell’azoto c’è il tiofene (C4H4S). Ha proprietà molto simili al benzene e si trova in bassa percentuale nel petrolio. Trova applicazioni nelle aziende farmacologiche e nell’industria delle plastiche per realizzare il politiofene. un polimero con buona conducibilità.
Le reazioni degli idrocarburi aromatici
Come già detto i composti aromatici reagiscono facilmente con atomi o molecole elettrofile per dare luogo a reazioni di sostituzione. La dinamica vede un atomo di idrogeno dell’anello ciclico venire rimpiazzato con un atomo o un gruppo sostituente diverso. Una delle sostituzioni più comuni è l’alogenazione e in particolare la clorurazione del benzene.
Un’altra reazione di sostituzione comune delle molecole aromatiche è l’alchilazione, dove un gruppo metilico o etilico prende il posto di un atomo di idrogeno. Per esempio facendo reagire il benzene con il cloruro di metile si ottengono come prodotti acido cloridrico e toluene (metil-benzene).
I composti organici si possono ossidare a livello di una catena laterale, per esempio un gruppo metilico o etilico, in presenza di permanganato di potassio (KMnO₄). Questo trasforma la catena laterale in un acido carbossilico (-COOH).