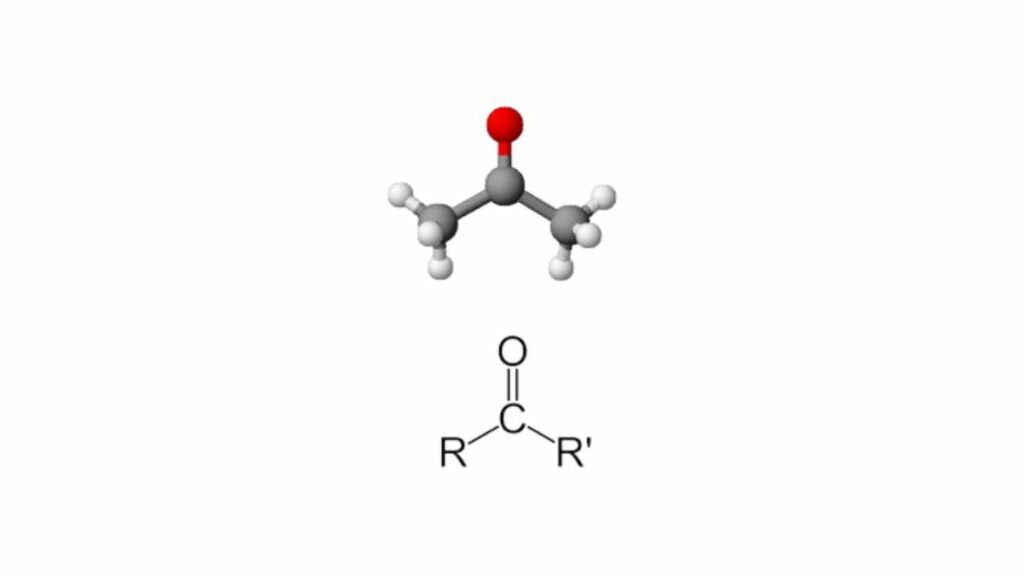
La struttura dei corpi chetonici
Tra le classi di composti organici quella dei chetoni non è tra le più semplici da studiare poiché la loro struttura è molto simile a quella di un altro gruppo, le aldeidi. Entrambi presentano nella struttura molecolare un gruppo carbonilico, ma nel caso delle aldeidi il carbonio su cui si inserisce è legato anche a un atomo di idrogeno.
Questi composti nel corpo umano prendono il nome di corpi chetonici e derivano dal metabolismo dei lipidi. Si accumulano nel fegato come substrato di riserva per ricavare glucosio in caso di periodi di digiuno prolungato. In chi soffre di diabete la loro concentrazione tende ad aumentare fino a diventare pericolosa.
Le proprietà dei chetoni
Sono ossia formati da catene di atomi di carbonio di cui uno presenta un doppio legame con un atomo di ossigeno. I due legami possibili rimanenti li fa con i carboni adiacenti, quindi non legame atomi di idrogeno. Uno dei più noti è l’acetone, la più semplice di queste molecole (C3H6O).
Non si tratta i composti facilmente solubili in acqua e alla vista appaiono incolori, ma hanno un odore caratteristico molto pungente. Alcuni chetoni sono prodotti all’interno dell’organismo, tra cui proprio l’acetone che però di solito è presente in concentrazioni minime. In presenza di determinate patologie del metabolismo però queste possono aumentare.
Anche alcuni tipologie di fermentazione possono portare alla produzione di questi composti, che si usano come ingrediente negli olii essenziali. Quando le loro catene si fanno molto elaborate e pesanti (sopra i 12 atomi di carbonio) possiamo trovarli sotto forma di solidi cristallini. Sono solubili nell’alcol, ma non nei solventi apolari come il benzene.
Come funziona la nomenclatura
Come già suggerito al paragrafo precedente, per dare il nome ai chetoni il suffisso da aggiungere è -one. Quando si ha di fronte la struttura della molecola come sempre in Chimica Organica si cerca la catena di atomi di carbonio più lunga. Questa deve contenere il gruppo C = O che non deve essere a una delle estremità (altrimenti ci troveremmo di fronte a un’aldeide).
Una volta scelta la catena si numerano i carboni partendo dall’estremità più vicina al gruppo carbonilico. Per i sostituenti si seguono le classiche regola della nomenclatura IUPAC. Vediamo come esempio la molecola del 2-butanone: deve avere una catena di 4 carboni dove C = O è ils secondo carbonio. Dunque la molecola sarà CH3COCH2CH3.
Passiamo ora a un paio di chetoni che presentano una catena di carboni più lunga, come il 3-pentanone. Il nome del composto ci dice che il gruppo C = O è il terzo di cinque carboni, dunque la molecola presenta una simmetria. Si tratta infatti del carbonio centrale (è il terzo sia da sinistra che da destra) e la formula che risulta è CH3CH2OCH2CH3.
Questi composti possono presentarsi anche in forma ciclica (es. ciclopentanone) dove il doppio legame con l’ossigeno viene disegnato esternamente all’anello. Alcuni sono derivati del benzene, come l’acetofenone o il difenilchetone, dove due anelli aromatici sono collegati da un gruppo carbonilico.
Le reazioni e la sintesi dei chetoni
Si tratta di una reazione reversibile, in quanto gli alcoli secondari si possono ricavare effettuando un’idrogenazione (riducendo anziché ossidando). Come catalizzatori si possono usare metalli come il nichel o il palladio. Se invece si portano i chetoni in ambiente basico si possono ottenere degli alcani con una reazione detta riduzione di Wolff-Kishner.
Per catalizzare questa reazione serve un composto binario dell’azoto detto niazina (formula N2H2N2H2) e l’idrossido di potassio (KOH). Come substrato di partenza si possono usare anche le aldeidi, ricavando sempre degli alcani. Il gruppo C = O inoltre reagisce con carbanioni detti reattivi di Grignard formando degli alcoli. Il più utilizzato è RMgX, dove RX è un alogenuro alchilico.
Se dopo l’azione del reattivo di Grignard si aggiunge una molecola d’acqua grazie alla sua idrolisi il carbonio a cui è legato l’ossigeno lega anche un idrogeno. Si forma così un gruppo -OH.