Numero quantico di spin nella struttura elettronica atomica
Capire il numero quantico di spin significa entrare nel cuore della descrizione dell’atomo in fisica moderna. Senza spin e senza il principio di esclusione, la tavola periodica non avrebbe alcun ordine riconoscibile. Gli elettroni sembrerebbero particelle identiche disposte a caso nello spazio energetico disponibile.
Con la nascita della meccanica quantistica, concetti come orbital e numeri quantici hanno sostituito le vecchie orbite planetarie di Bohr. Oggi descriviamo ogni elettrone con quattro numeri, e proprio quello legato allo spin giustifica la presenza di coppie elettroniche negli orbitali. Questo tema conta molto per chi studia chimica, fisica o discipline sanitarie, perché entra in ogni configurazione elettronica e in ogni legame chimico. Inoltre collega risultati sperimentali, come gli spettri atomici fini, con strumenti teorici avanzati.
In queste pagine vedremo perché il principio di esclusione di Pauli dipende dalla natura di fermione dell’elettrone, cosa rappresenta davvero lo spin e come il relativo numero quantico si inserisce nel quadro dei numeri quantici. Esploreremo esempi concreti, collegamenti con l’equazione di Schrödinger e con altre leggi fondamentali, mantenendo sempre un linguaggio chiaro ma rigoroso.
Dal modello classico al numero quantico di spin
Prima di affrontare il principio di esclusione, conviene ripercorrere il passaggio dal modello classico agli orbitali quantistici. All’inizio l’elettrone veniva immaginato come un pianeta che ruota attorno al nucleo, con traiettorie ben definite.
Con l’ipotesi di De Broglie e la costante di Planck, la materia assume anche natura ondulatoria. L’equazione di Schrödinger descrive allora stati di probabilità, non orbite rigide. Ogni stato è identificato da specifici numeri quantici, che definiscono energia, forma e orientazione degli orbitali. In questo quadro il numero quantico di spin aggiunge un grado di libertà intrinseco alla particella, indipendente dal moto nello spazio.
Osservazioni spettroscopiche dell’idrogeno, come il cosiddetto fine-structure, mostrarono sdoppiamenti di righe spiegabili solo introducendo lo spin. Anche i livelli energetici nei campi magnetici, analizzati nell’effetto Zeeman, confermarono l’esigenza di un momento magnetico interno.
Per chi studia oggi configurazioni elettroniche, questo passaggio storico non è solo curiosità. Permette di capire perché non possiamo ignorare lo spin quando costruiamo gli schemi degli atomi e perché alcune transizioni elettroniche sono permesse, mentre altre risultano vietate o fortemente sfavorite.
Numero quantico di spin e principio di esclusione
Il principio di esclusione di Pauli nasce per spiegare la struttura fine degli spettri atomici, ma va molto oltre. Esso afferma che due elettroni in un atomo non possono avere tutti e quattro i numeri quantici uguali.
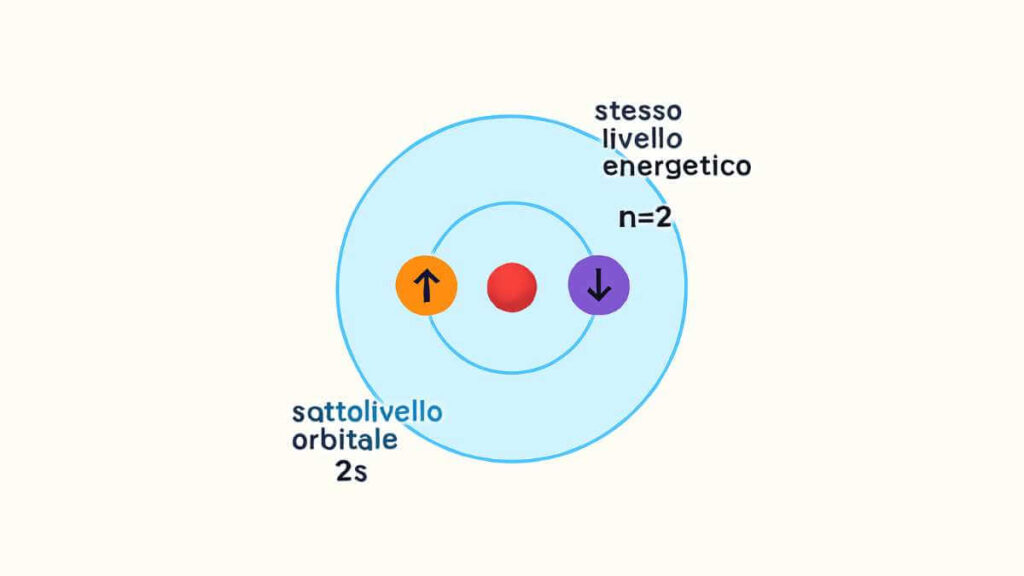
In pratica, uno stesso orbitale può ospitare al massimo due elettroni, e devono avere numero quantico di spin opposto.
Questa proprietà discende dal fatto che l’elettrone è un fermione, quindi obbedisce alle statistiche di Fermi-Dirac.
Particelle come il fotone, che sono bosoni, non rispettano l’esclusione e possono occupare lo stesso stato. La differenza spiega fenomeni macroscopici molto diversi, dal comportamento dei metalli alla luce laser.
Senza il principio di esclusione di Pauli, tutti gli elettroni cadrebbero nello stato energetico più basso, rendendo impossibile l’esistenza di chimica complessa.
I gusci elettronici degli atomi, le proprietà magnetiche dei materiali e perfino la stabilità della materia ordinaria dipendono da questa regola. Per questo, quando si studia il numero quantico di spin, non si affronta un dettaglio marginale, ma una proprietà strutturale che sostiene l’intera architettura della fisica della materia.
Definizione operativa del numero quantico di spin
Dal punto di vista formale, il numero quantico di spin descrive la componente lungo un asse del momento angolare intrinseco.
Per l’elettrone il modulo dello spin vale sempre \(s = \frac{1}{2}\), indipendentemente dallo stato energetico occupato.
Il numero quantico di spin – indicato con \(m_s\) – può assumere solo due valori: \(m_s = +\frac{1}{2}\) oppure \(m_s = -\frac{1}{2}\).
Questi corrispondono alle due possibili proiezioni dello spin su un asse scelto, spesso associato a un campo magnetico esterno. In un atomo ogni elettrone è quindi descritto da quattro numeri quantici principali. Ecco i principali elementi:
- numero quantico principale n, legato al livello energetico
- numero quantico secondario l, associato alla forma dell’orbitale
- numero quantico magnetico m_l, legato all’orientazione spaziale
- numero quantico di spin m_s, relativo alla proiezione dello spin
Questa classificazione non è un artificio matematico.
Permette di prevedere degenerazioni di livelli, regole di selezione e intensità delle righe spettrali. Nei calcoli di chimica quantistica, la scelta corretta delle configurazioni di spin riduce drasticamente il numero di stati da considerare. Di fatto, ogni volta che si scrive una configurazione elettronica, si usa implicitamente il numero quantico di spin, anche se non sempre lo si indica esplicitamente.
Spin, configurazioni elettroniche e regola di Hund
Quando si riempiono gli orbitali atomici, il numero quantico di spin guida la disposizione degli elettroni insieme alla regola di Hund. Questa regola afferma che, a parità di energia, la configurazione con il massimo numero di elettroni spaiati è favorita.
Consideriamo, per esempio, il riempimento degli orbitali p nel carbonio.
Secondo la regola di Hund, i tre orbitali p vengono occupati da tre elettroni con numero quantico di spin parallelo prima di formare coppie. Questa scelta massimizza il momento magnetico totale e riduce la repulsione elettronica.
Nei corsi universitari di chimica inorganica, esercizi ripetuti mostrano come piccole variazioni nelle coppie di spin modifichino il magnetismo di un complesso metallico.
Anche la stabilità relativa di configurazioni ad alta o bassa spin nei metalli di transizione si interpreta in questo schema. In tutti questi casi, il comportamento reale delle sostanze conferma con elevata precisione le previsioni fondate sul principio di esclusione e sui numeri quantici di spin, rendendo operativi concetti apparentemente astratti.
Relazione tra spin, equazioni fondamentali e limiti di misura
Lo spin non è solo un’etichetta introdotta a posteriori: emerge naturalmente da teorie più generali.
L’equazione di Dirac, che unisce meccanica quantistica e relatività ristretta, prevede lo spin dell’elettrone e il suo momento magnetico in modo automatico.
Nel limite non relativistico, i risultati dell’equazione di Dirac tornano compatibili con l’equazione di Schrödinger, ma il numero quantico di spin resta indispensabile.
Esperimenti di scattering su fasci di elettroni e misure di risonanza di spin elettronico mostrano deviazioni quantizzate, impossibili da spiegare con un modello puramente classico.
Qui entra in gioco anche il principio di indeterminazione di Heisenberg: non possiamo misurare simultaneamente con precisione assoluta componenti diverse del momento angolare di spin.
Allo stesso tempo il principio di sovrapposizione consente stati combinati di spin up e spin down, base di tecnologie come i qubit.
Rispetto a leggi classiche continue, come la legge di Poiseuille nei fluidi, lo spin introduce discreti salti di stato. Questa discrezione rende i sistemi quantistici al tempo stesso fragili e controllabili, aprendo la strada all’informazione quantistica.
Lo spin come filo conduttore tra microcosmo e tecnologia
Vista nel suo insieme, la teoria del numero quantico di spin mostra una coerenza sorprendente. Dalle righe spettrali degli atomi alla stabilità delle stelle nane bianche, il principio di esclusione di Pauli e lo spin governano strutture che vanno ben oltre il laboratorio di fisica.
Nel percorso che collega numeri quantici, configurazioni elettroniche, equazione di Dirac e proprietà magnetiche dei materiali, il numero quantico di spin agisce come filo invisibile ma essenziale.
Le tecnologie basate su fenomeni di spin, dalla risonanza magnetica alle memorie spintroniche, sfruttano direttamente questa proprietà quantistica. Anche quando il linguaggio della teoria sembra astratto, i risultati appaiono quotidianamente in strumenti medici, dispositivi elettronici e metodi di indagine sui materiali.
Comprendere davvero lo spin significa quindi riconoscere quanto profondamente il mondo quantistico plasmi il reale.
La fisica degli elettroni non resta confinata nelle equazioni; diventa struttura, colore, materia, informazione. Ed è proprio in questa continuità tra teoria ed esperienza che il principio di esclusione continua a rivelare la sua forza concettuale.