Le vie metaboliche e le gluconeogenesi
Parlando delle vie metaboliche spesso si trascurano quelle dell’anabolismo, come la gluconeogenesi. Si tratta di un processo finalizzato a produrre glucosio quando quello assunto dagli alimenti risulta insufficiente e quindi la sua concentrazione cala nel flusso ematico. Per ottenere zuccheri questo processo parte da precursori non glucidici, come gli amminoacidi o il glicogeno.
Questo composto si produce quando il glucosio assunto con la dieta supera le necessità dell’organismo e occorre immagazzinarlo. Il glicogeno infatti è un polisaccaride che funge da riserva energetica e si accumula all’interno del fegato e nei muscoli scheletrici. Si tratta di una riserva che va periodicamente ripristinata dopo sforzi fisici prolungati assumendo zuccheri.
Le finalità della gluconeogenesi e cosa la stimola
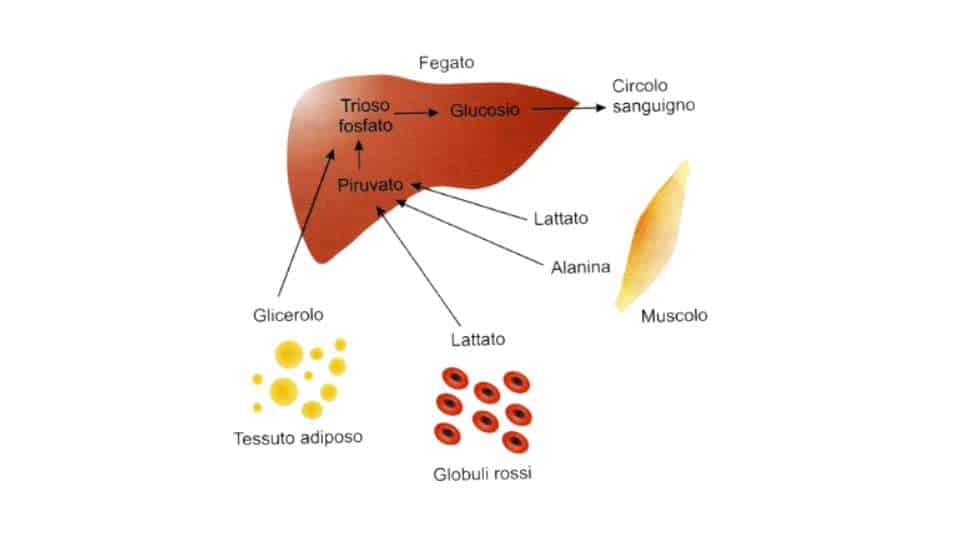
Questo processo negli animali risulta particolarmente attivo all’interno delle cellule epatiche per le ragioni già descritte nell’introduzione. Il glucosio che si produce nel fegato si può poi trasportare per via ematica agli organi che lo richiedono. Nell’organismo l’organo che consuma più glucosio è il cervello, che ne richiede circa 120 grammi al giorno.
Dato che tra i precursori usati da questa via metabolica c’è anche il lattato la gluconeogenesi aiuta ad abbassarne la concentrazione. Sopra una certa soglia infatti questo può diventare tossico per l’organismo se inizia ad accumularsi nella circolazione sanguigna. Deriva dall’acido lattico prodotto nei muscoli durante i processi anaerobici o sforzi prolungati in carenza di ossigeno.
A richiedere l’attivazione del processo di produzione di glucosio può essere anche un eccesso nell’assunzione di amminoacidi con la dieta. Escludendo la licina e la leusina infatti tutti gli altri possono diventare substrati di partenza per produrre zuccheri. In genere li si converte in intermedi del ciclo dell’acido citrico rimuovendo l’azoto dalla loro struttura.
L’organismo ricorre a questa via anche come meccanismo di sopravvivenza se si trova in condizioni di digiuno prolungato. Una situazione che si configura quando non si assumono zuccheri per due o tre giorni, sufficienti a eliminare anche le riserve di glicogeno. Anche la dieta chetogenica richiede questo processo in quanto porta ad assumere prevalentemente proteine e grassi.
Le tappe enzimatiche per la sintesi del glucosio
Per prima cosa va detto che nonostante siano effettivamente processi opposti la gluconeogenesi non segue le tappe della glicolisi a ritroso. Ci sono delle “deviazioni” necessarie per evitare investimenti energetici in una situazione dove l’organismo è a digiuno. Sette delle dieci reazioni necessarie per arrivare al glucosio però sono in comune.
La prima divergenza corrisponde al primo passaggio, dove a partire dal piruvato si ottiene il fosfoenolpiruvato. Questo richiede due enzimi: la piruvato carbossilasi e la PEP carbossichinasi. La prima produce l’ossalacetato, a cui poi si aggiunge un gruppo fosfato a partire da una molecola di GTP, che dopo la reazione risulta nella forma GDP. Il sistema della doppia reazione permette l’attivazione del piruvato.
La seconda tappa specifica della gluconeogenesi vede l’intervento dell’enzima fruttosio 1,6 bifosfatasi. che permette la formazione di fruttosio 6-fosfato. La regolazione dell’attività di questo enzima è mediata in via allosterica dal citrato e richiede l’apporto di una molecola d’acqua. La glicolisi invece formava fruttosio 1,6 bifosfato usando ATP.
Per finire la terza e ultima differenza fra i due processi è a livello della reazione finale, ovvero quella che si conclude con la sintesi del glucosio. Il passaggio da glucosio 6-fosfato a glucosio è catalizzato dall’enzima glucosio 6-fosfatasi, che come l’enzima del passaggio descritto prima richiede una molecola d’acqua. Durante la reazione si forma l’intermedio fosfoistidina.
Malattie che influenzano la gluconeogenesi
A meno che non avvenga almeno una di queste il paziente risulta asintomatico. La carenza dell’enzima infatti diventa manifesta solo nei casi in cui si rende necessaria. Di conseguenza il trattamento corrisponde all’evitare situazioni di digiuno prolungato e a non prevedere nella propria dieta gli zuccheri sopra nominati. Crescendo per fortuna chi soffre di questo deficit inizia a sviluppare una maggiore tolleranza.
Un altro disturbo che può interferire con la gluconeogenesi è la malattia di Von Gierke, detta anche glicogenosi di tipo I. Chi ne soffre accumula più glicogeno del normale in quanto non è in grado di utilizzare gli zuccheri. Gli effetti di questa patologia infatti bloccano l’azione dell’enzima glucosio-6-fosfatasi, impedendo la produzione di glucosio a partire dal glicogeno.
Anche chi soffre di questa malattia dunque rischia una grave ipoglicemia durante i periodi di digiuno. L’accumulo eccessivo di glicogeno a livello del fegato e dei reni però può avere anche altre conseguenza gravi sull’organismo. Uno dei sintomi che devono mettere in allarme sono le dimensioni del fegato, che in questi pazienti spesso appare ingrossato.